A kis háztartási gépek széles körű elterjedése a fogyasztók által áramforrások, vagyis egyetlen tápellátású áramkörök szükségességét vonja maga után. galváncellák, közismert nevén elemek. Először 1800-ban jelentek meg, Alessandro Volta olasz fizikusnak köszönhetően. Méretükben és alakjukban, feszültségükben, kapacitásukban és elemtípusukban is különböznek. Az alkáli és sós elemeket széles körben használják a kisgépek és az elektronikai piacon.
Mik azok a sós elemek?
Sóakkumulátorok — egyszerű eszközökben kémiai reakció révén keletkező elektromos áram forrásai. Ezeket néha szén-cink vagy szén elemeknek is nevezik. Ez a típusú cella a legolcsóbbnak számít, de alacsony energiasűrűségű, így jól alkalmas kis fogyasztású eszközökhöz. Nagy energiafogyasztású vagy a terhelési áram és a hőmérséklet jellegzetes túlfeszültségével járó eszközökben nem sokáig tartanak, ezért nem használják őket.
Sóakkumulátorok kijelölése
A sóoldatos akkumulátorok megjelölését több szabvány szerint fogadják el:
- Amerikai osztályozási rendszer.
- Nemzetközi rendszer (IEC).
- Államközi szabvány (GOST).
| Amerikai osztályozási rendszer | Nemzetközi Osztályozás IEC | GOST | Méret, mm | Kapacitás, mAh |
| Egy | R23 | 17x50 | ||
| AA | R6 | 316 | 14,5x50,5 | 1100 |
| AAA | R03 | 286 | 10,5x44,5 | 540 |
| C | R14 | 343 | 26,2x50 | 3800 |
| D | R20 | 373 | 34,2x61,5 | 8000 |
| F | R25 | 33x91 | ||
| 1/2AA elem | 14250 rand | 312 | 14,5x25 | 250 |
| R10 | R10 | 332 | 21,5x37,3 | 1800 |
Például egy sóoldatos akkumulátor R 6 jelölése a következőt jelenti: kerek, hengeres, ujj, só típusú elem, teljes méretek 14,5x50,5, kapacitás1100 mAh. A szabványfeszültség 1,5 V. Az akkumulátor címkéjén található „R” jelölés (só) megkülönbözteti a sóoldatos elemeket más típusú elemektől (alkáli vagy lítium).
Tervezés és kompozíció
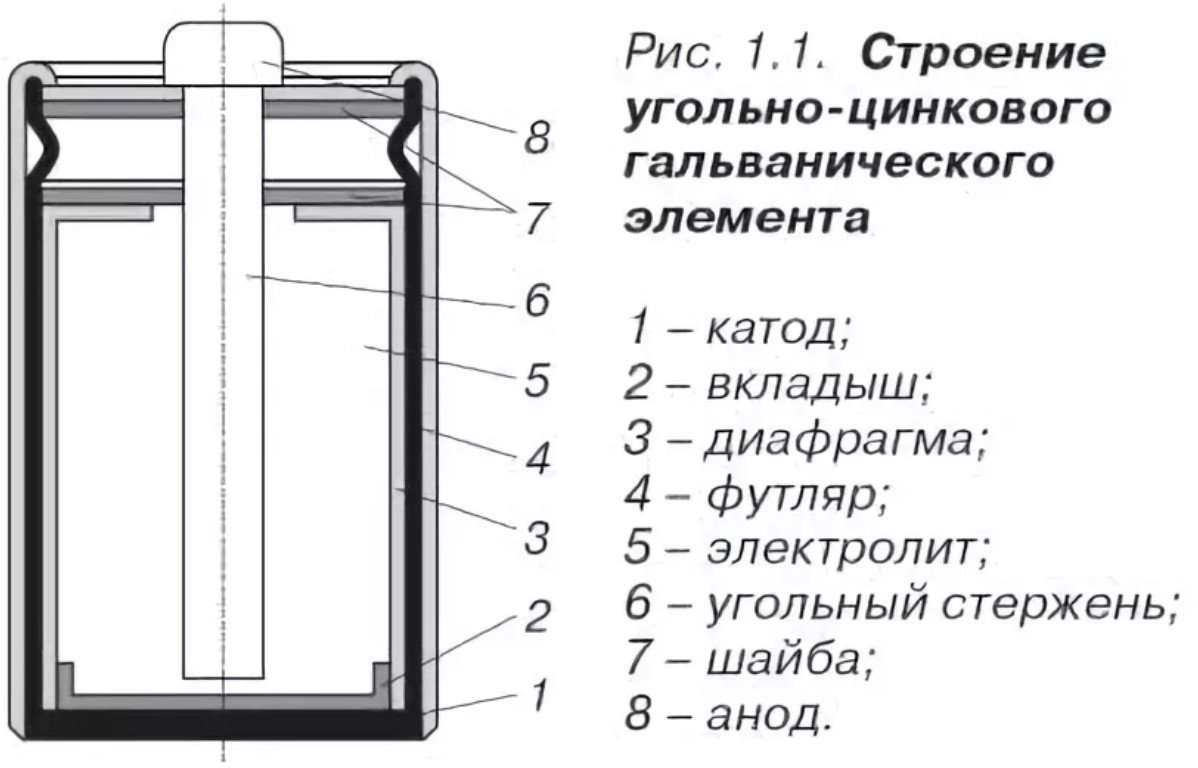
A só akkumulátor kialakítása meglehetősen egyszerű, és a következőkből áll:
- Katód - ugyanaz a só akkumulátor tokja készült cinkből készült, javított korróziógátló tulajdonságokkal és magas tisztítási fokú (mínusz).
- Az anód egy préseléssel előállított agglomerátum, elektrolittal (plusz) impregnálva.
- Elektrolit: ammónium-klorid vagy cink-klorid, sűrítőanyag (keményítő) hozzáadásával.
- Szénáramvezető - áthalad a központon, paraffinösszetétellel kezelve.
- Gázkamra - a tetején található, a kémiai reakcióból származó gázok összegyűjtésére szolgál.
- Tömítés - a tetején található, tömítőanyagként működik.
- Védőtok - karton vagy fém a korrózió és az elektrolitszivárgás elleni védelemre.
Vizsgáljuk meg egy sóoldatos akkumulátor összetételét kémiai szempontból:
- A katód nagy tisztaságú cink, amely ellenáll a korróziónak.
- Anód - MnO keverék2, grafit, elektrolit impregnálás.
- Az elektrolit ammónium-klorid, vagy cink-klorid és kalcium-klorid keveréke.
Melyik elemek jobbak: sós (1) vagy alkáli (2)?
Az összehasonlítás táblázat formájában is elvégezhető, ahol a különböző típusú elemek előnyei és hátrányai jól láthatóak:
| Összehasonlítási paraméterek | 1 | 2 |
| Hőmérsékleti viszonyok, üzemi feltételek | Alacsony hőmérsékleten a teljesítmény csökken, és nem bírja az áramingadozásokat. | Alacsony hőmérsékleten is jól működik - akár -20 fokigÓkönnyen ellenállnak a túlfeszültségeknek, nem félnek a terhelési áram hirtelen növekedésétől |
| Minőségét megőrzi (nap/hónap/év): | 2-3 év | 5 év |
| Alkalmazás | Alacsony áramfogyasztású eszközökben használható | Közepes és nagy energiafogyasztású berendezésekben használható |
| Műszerek, műszaki eszközök | Ébresztőórák, faliórák, távirányítók, mini zseblámpák, egyszerű játékok | Lejátszók, zseblámpák, zenélő játékok, hangrögzítők, vérnyomásmérők |
Amikor egy adott működési követelményekkel rendelkező eszközhöz áramforrást választunk, fontos tudni, hogyan lehet különbséget tenni a sóoldatos és az alkáli elemek között. Míg a sóoldatos elemeket R betű jelöli, az alkáli elemeket L (LR) betű előzi meg.
Következtetések és ajánlások
Ez a fajta áramforrás könnyebb és megfizethetőbb. A sóoldatos elemek eltarthatósága azonban rövid – 2-3 év –, és tárolás, valamint használat közben hirtelen áramlökés esetén részleges önkisülés következhet be bennük. Ezért, tekintettel viszonylag gyenge teljesítményükre, de viszonylag alacsony árukra, könnyű több készlet elemet vásárolni tartalékként.
Nem magas kapacitássóelemek (2-3-szor kevesebb, mint más típusúak) korlátozza használatukat egyszerű, alacsony terhelési áramú eszközökre.
Könnyű megállapítani, hogy tölthetők-e sóoldatos akkumulátorok: az akkumulátor neve fel van tüntetve a töltendő eszköz házán. kapacitásmAh-ban. Ha ez az érték nem áll rendelkezésre, akkor egy hagyományos akkumulátorról van szó, és számos szakértői tanács ellenére sem szabad tölteni. A töltés nem biztosítja a várt hosszú távú hatást, és túlmelegedés, valamint elektrolitszivárgás miatt balesetet okozhat. Ha megbízhatóbb, tartósabb áramforrásra van szüksége, érdemesebb alkáli alternatívába vagy újratölthető akkumulátorba fektetni.
Érdekes tény: Sóakkumulátor saját kezűleg Nagyon egyszerűen elkészíthető. Szükséged lesz 50 kopejkás érmékre, fóliára, papírra és sóoldatra. Használat előtt a legjobb, ha az érméket ecetoldatba áztatod, hogy eltávolítsd a lepedéket vagy a szennyeződéseket. Szereld össze az eszközt: egy érme, a sóoldatba áztatott papír és fólia. Ismételd meg ezt a folyamatot többször, egy oszlopot hozva létre, amelynek egyik végén az érme (pozitív), a másikon pedig a fólia (negatív) található. Az áramot az elektrolit (sóoldat) által a fólia féme és az érme között létrehozott potenciálkülönbség hozza létre. Ezt a találmányt Volta-oszlopnak nevezik, és feszültsége közvetlenül függ a felhasznált érmék számától: minél több érme van, annál nagyobb a kapott feszültség. A kísérlet után azonban az érmék már nem használhatók; rozsdás bevonat lesz rajtuk.